近日,我校亚洲无码av
刘润辉教授团队报道了一种用于骨修复的基于仿生海藻酸钠/α-TCP有机-无机互穿网络的力学性能增强型微球。该研究成果以“Bioinspired Alginate/α-TCP Organic-Inorganic Interpenetrating Network Microspheres for Bone Repair”为题发表在Advanced Functional Materials上(10.1002/adfm.202524421)。
基于骨水泥的微创再生疗法在骨缺损修复领域具有重要应用价值。聚甲基丙烯酸甲酯(PMMA)和磷酸钙骨水泥(CPC)是最常见的两种骨水泥。然而,PMMA骨水泥存在不可降解、不可吸收,以及在体内凝固时放热过多等固有缺陷。尽管CPC的成分与天然骨相似,但其力学性能较差、易溃散等缺点限制了实际应用。且这些可注射型骨水泥通常缺乏孔隙率,不利于细胞和血管的长入从而影响骨修复效果。近年来,微球化骨修复材料因其独特的优势备受关注。微球化骨水泥能够以最小侵入创口填充任何几何形状的缺损,并且自然堆叠的微球之间会形成微米级的孔隙。这些孔隙为内源性细胞提供了迁入和营养代谢的通道,同时有助于血管网络的形成。然而,现有单一组分体系如水凝胶或磷酸钙微球难以实现理想的骨修复效果。
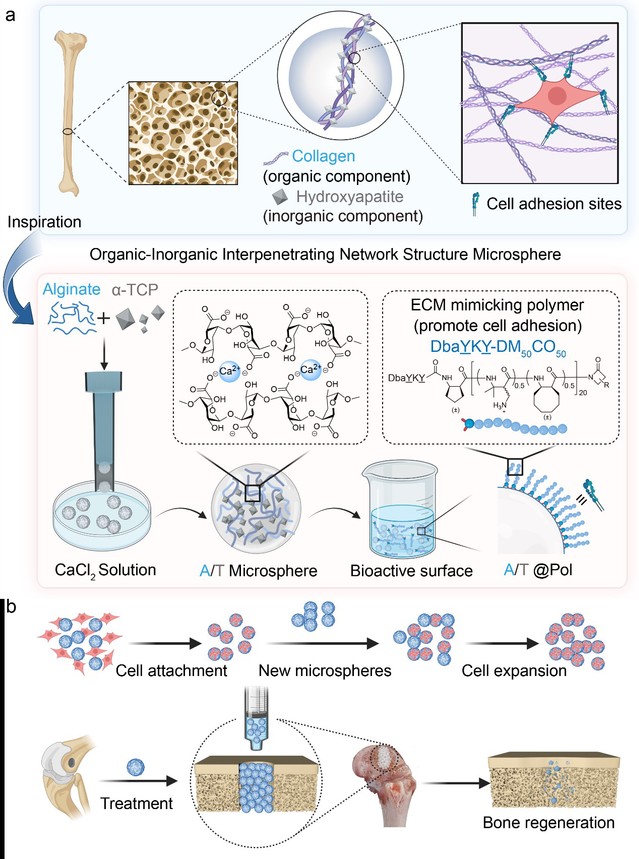
该研究选用α-磷酸三钙(α-TCP)作为无机组分,因其水合反应可在生理pH值条件下进行;且其水解生成的缺钙羟基磷灰石(CDHA)在晶体结构、化学组成和形态特征上与天然骨矿物更为接近。同时选用具有安全无毒的海藻酸钠(Alg)作为有机组分。值得注意的是,α-TCP释放的Ca2+不仅能促进缺损部位的矿化过程,还可作为海藻酸钠凝胶化的可靠钙源,从而确保复合材料的稳定性。该研究通过一步离心法制备了粒径均一可控的Alg/α-TCP复合微球,该微球具有天然骨相似的有机-无机互穿网络结构。为进一步模拟细胞外基质(ECM)蛋白中的细胞粘附位点,该研究采用近期发现具有促进细胞粘附功能的阳离子-两亲性β-氨基酸聚合物DbaYKY-DM50CO50对微球表面进行修饰。体外实验表明,经修饰的Alg/α-TCP复合微球能有效支持细胞粘附、增殖,并实现一体化的细胞冻存、复苏与扩增。在大鼠股骨缺损模型中,该微球展现出优异的骨修复效果。
华东理工大学研究生窦蒙悦是该论文的第一作者,刘润辉教授和陈琦特聘副研究员为通讯作者。该研究得到了国家自然科学基金委、材料生物学与动态化学教育部前沿科学中心等基金的资助。
论文链接://doi.org/10.1002/adfm.202524421
